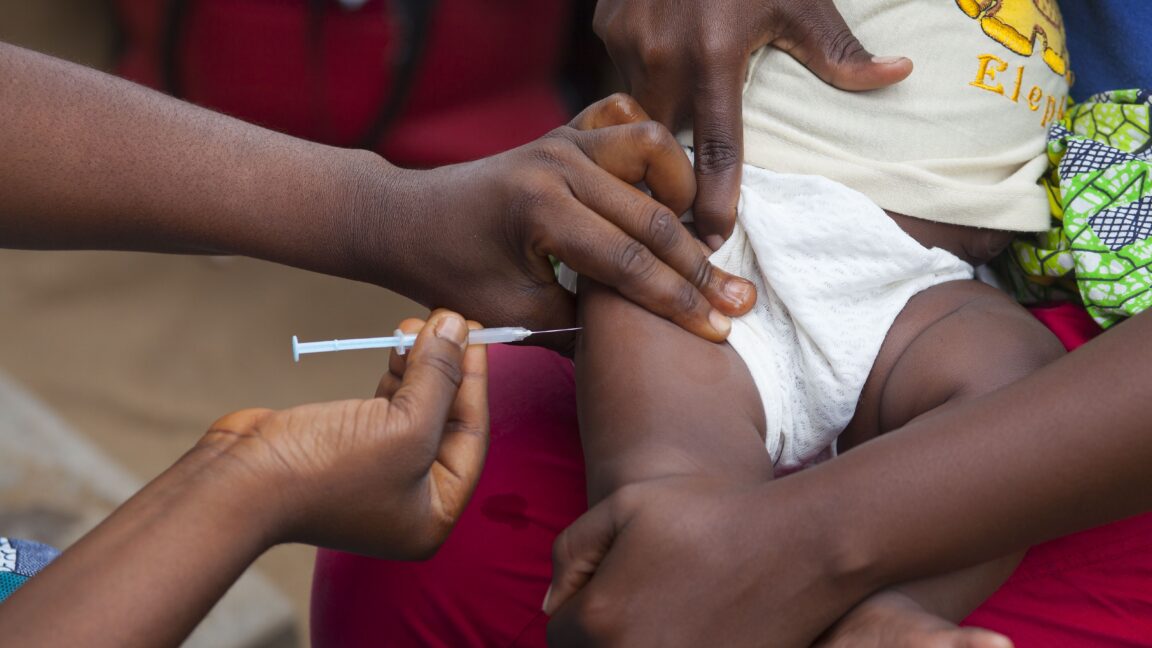
L’OMS dénonce un essai vaccinal américain sur des nouveau-nés comme étant « contraire à l’éthique »
L’Organisation mondiale de la santé a publié vendredi une déclaration formelle dénonçant un essai vaccinal financé par les États-Unis comme étant « contraire à l’éthique », car il priverait certains nouveau-nés de Guinée-Bissau, en Afrique, d’un vaccin établi, sûr et potentiellement salvateur contre l’hépatite B.
« Sous sa forme actuelle et sur la base des informations accessibles au public, l’essai n’est pas conforme aux principes éthiques et scientifiques établis », a conclu l’OMS, après avoir fourni une liste à puces des raisons pour lesquelles l’essai était nocif et de mauvaise qualité.
L’essai a suscité une condamnation généralisée de la part d’experts en santé depuis que l’avis de financement américain a été publié dans le Federal Register en décembre. L’avis révélait que les Centers for Disease Control and Prevention – sous la direction du secrétaire à la Santé anti-vaccin Robert F. Kennedy Jr. – avaient accordé 1,6 million de dollars à des chercheurs danois pour leur proposition non sollicitée et non concurrentielle de mener l’essai.
Les chercheurs danois sont dirigés par Christine Stabell Benn et son mari Peter Aaby du Bandim Health Project, basé à l’Université du Danemark du Sud à Copenhague. Benn et ses collègues sont depuis longtemps controversés pour leurs pratiques douteuses dans la recherche sur de présumés problèmes de sécurité vaccinale. Kennedy a cité leurs travaux dans sa décision de réduire le financement mondial des vaccins.
Le financement par le CDC de l’essai sur le vaccin contre l’hépatite B de Benn est également intervenu peu après que les conseillers de l’agence – choisis personnellement par Kennedy – ont décidé d’abandonner une recommandation universelle de longue date pour une dose de vaccin contre l’hépatite B à la naissance. Cette décision a été largement décriée par les experts en santé.
Dans l’essai en Guinée-Bissau, l’équipe de Benn prévoyait de randomiser 14 000 nouveau-nés pour qu’ils reçoivent leur première dose de vaccin contre l’hépatite B soit à la naissance, soit à six semaines, puis d’étudier les différences dans les résultats présumés en matière de sécurité. Actuellement, la Guinée-Bissau administre la première dose de vaccin à six semaines, mais a déjà décidé de passer à une recommandation d’une dose à la naissance en 2028. La raison du retard de mise en œuvre est due à des contraintes de ressources.
« Exploiter la pénurie n’est pas éthique », a écrit l’OMS dans sa déclaration d’aujourd’hui.
Essai dangereux
L’agence de santé des Nations Unies a souligné que la dose de vaccin contre l’hépatite B à la naissance est « une intervention de santé publique efficace et essentielle » qui « est utilisée depuis plus de trois décennies, avec plus de 115 pays l’incluant dans leurs calendriers nationaux. »
« Elle prévient les maladies hépatiques potentiellement mortelles en stoppant la transmission de la mère à l’enfant à la naissance », a écrit l’OMS, notant que plus de 12 pour cent des adultes en Guinée-Bissau ont une hépatite B chronique.
Dans une section sous-titrée « Pourquoi priver du vaccin est contraire à l’éthique », l’OMS expose toutes les raisons pour lesquelles l’essai est dangereux.
« D’après ce qui est décrit publiquement, le protocole ne semble pas garantir même un niveau minimum de réduction des dommages et de bénéfice pour les participants à l’étude (par exemple, dépister les femmes enceintes et vacciner les nouveau-nés exposés à l’hépatite B) », a écrit l’OMS.
En tant que vaccin salvateur éprouvé, le retenir à certains participants à l’étude exposerait les nouveau-nés à des dommages graves et potentiellement irréversibles, notamment une infection chronique, une cirrhose et un cancer du foie, soutient l’OMS. Il n’y a aucune justification scientifique pour retenir une intervention éprouvée, et il n’existe aucune preuve crédible des problèmes de sécurité que Benn et ses collègues prétendent rechercher dans leur essai. L’OMS a également noté que les informations accessibles au public sur l’essai indiquent qu’il sera en simple aveugle, sans groupe témoin traité, ce qui « soulève une probabilité importante d’un risque substantiel de biais, limitant l’interprétabilité des résultats de l’étude et leur pertinence politique ».
À l’heure actuelle, l’essai semble être suspendu. Nature News a rapporté que lors d’une conférence de presse le 22 janvier, des responsables de la santé en Guinée-Bissau ont déclaré qu’un examen technique et éthique était en attente. « Il n’y a pas eu de coordination suffisante pour prendre une décision finale concernant l’étude », a déclaré Quinhin Nantote, ministre de la Santé publique de la Guinée-Bissau. « Face à cette situation, nous avons décidé de la suspendre. »
Auparavant, les Centres africains de contrôle et de prévention des maladies avaient suggéré que l’essai n’irait pas de l’avant. Cependant, le Département américain de la Santé et des Services sociaux a fourni une déclaration indiquant qu’il se déroulait « comme prévu ».